Eurofins U.S. Clinical Diagnostics Network reçoit une autorisation d'utilisation d'urgence pour son test COVID-19 à domicil...
19 Octobre 2020 - 11:33AM
Business Wire
Le test PCR nasal At Home COVID-19 est facile à
utiliser et indolore
Eurofins U.S. Clinical Diagnostics, a annoncé que Clinical
Enterprise Inc. a reçu une autorisation d'utilisation d'urgence
(EUA) de la Food and Drug Administration (FDA) américaine pour son
test PCR nasal COVID-19 à domicile. Le kit d'autocollecte agréé EUA
permet aux consommateurs d'effectuer un test peu invasif, pratique
et rapide confortablement chez eux. Les résultats sont fournis par
courrier électronique dans les 24 heures suivant la réception de
l'échantillon.
Disponible auprès de l'entreprise de vente directe aux
consommateurs d'Eurofins, empowerDX, le test à domicile peut
être commandé en ligne (https://empowerdxlab.com/) pour 89 USD.
Après avoir rempli un questionnaire, les clients recevront le kit
de prélèvement d'échantillons par FedEx.
Le centre d'excellence d'Eurofins spécialisé dans les maladies
infectieuses, Viracor, a conçu ce test en se basant sur le test
RT-PCR SARS-CoV-2, hautement sensible, agréé EUA par la FDA.
Eurofins U.S. Clinical Diagnostics Network est à l'avant-garde
des tests COVID-19 et a lancé son premier test RT-PCR pour le
SARS-CoV-2 le 13 mars dernier. Eurofins a depuis déployé plusieurs
tests très sensibles et spécifiques auprès de milliers de clients à
travers le pays, notamment des hôpitaux, des cabinets médicaux, des
maisons de retraite, des agences gouvernementales, des
organisations sportives et des employeurs. Le test At-home COVID-19
apporte une capacité supplémentaire à un catalogue déjà très
complet de tests, comprenant des tests groupés, des tests
d'anticorps, des tests sur les eaux usées, des tests sur les
masques usagés et bientôt des tests de salive.
Dans la lignée des innovations en cours dans le domaine des
tests COVID-19, Eurofins a renforcé les capacités de son réseau de
laboratoires afin de garantir un délai de traitement constant si le
nombre d'infections par COVID-19 devait continuer à augmenter dans
les semaines à venir. Depuis mars, la capacité de test d'Eurofins
US Clinical Diagnostics est passée à plus de 500 000 échantillons
par semaine. Le délai de communication des résultats a été en
moyenne de moins de 18 heures à compter de la réception des
échantillons au laboratoire.
Le test PCR nasal At Home COVID-19 n'est actuellement pas
disponible dans les États de New York, du New Jersey, du Rhode
Island et du Maryland.
Ce kit de collecte à domicile n'a pas été approuvé par la FDA ;
il a cependant été autorisé par la FDA dans le cadre d'un EUA
uniquement pour l'auto-collecte et la conservation d'échantillons
de prélèvement nasal en tant qu'aide à la détection d'acide
nucléique provenant du SRAS-CoV-2, et non pas pour d'autres virus
ou agents pathogènes, et uniquement pour la durée de la déclaration
de l'existence de circonstances justifiant l'autorisation d'une
utilisation d'urgence dans des dispositifs médicaux pendant
l'épidémie de COVID-19 conformément à la section 64(b)(1) de la loi
fédérale sur les aliments, les médicaments et les cosmétiques, 21
U. S.C. § 360bbb-3(b)(1), à moins que l'autorisation ne soit
résiliée ou révoquée plus tôt.
Le texte du communiqué issu d’une traduction ne doit d’aucune
manière être considéré comme officiel. La seule version du
communiqué qui fasse foi est celle du communiqué dans sa langue
d’origine. La traduction devra toujours être confrontée au texte
source, qui fera jurisprudence.
Consultez la
version source sur businesswire.com : https://www.businesswire.com/news/home/20201019005351/fr/
Matt Urbanek ir@eurofins.com
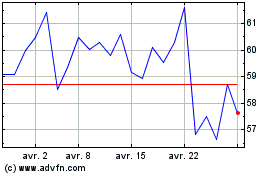
Eurofins Scientific (EU:ERF)
Graphique Historique de l'Action
De Mar 2024 à Avr 2024
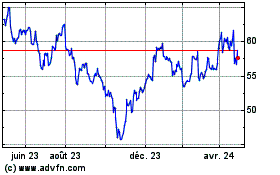
Eurofins Scientific (EU:ERF)
Graphique Historique de l'Action
De Avr 2023 à Avr 2024