GENFIT :
Lancement aux États-Unis d'une étude de Phase 2 initiée par un
investigateur, évaluant nitazoxanide chez des patients avec fibrose
NASH
-
Étude de phase 2 ciblant une
population de patients atteints de NASH avec fibrose de stade 2 ou
3
-
Effet anti-fibrotique de
nitazoxanide évalué par différentes approches, dont une méthode
innovante permettant de quantifier les taux de fibrogenèse
hépatique
Lille (France),
Cambridge (Massachusetts, États-Unis), le 3 décembre 2018 -
GENFIT (Euronext : GNFT - ISIN : FR0004163111), société
biopharmaceutique focalisée sur la découverte et le développement
de solutions thérapeutiques et diagnostiques dans le domaine des
maladies du foie, notamment d'origine métabolique, et des maladies
hépato-biliaires a annoncé aujourd'hui le lancement d'un essai
clinique de Phase 2 de preuve de concept évaluant nitazoxanide
(NTZ) chez des patients atteints de fibrose induite par la
stéatohépatite non-alcoolique (NASH), suite à la soumission du
protocole d'étude par le Pinnacle Clinical Research auprès de la
Food and Drug Administration américaine (FDA) .
Le Dr Stephen Harrison, Directeur
Médical du Pinnacle Clinical Research à San Antonio, Texas,
États-Unis, Professeur d'Hépatologie, Radcliffe College of
Medicine, Université d'Oxford, mènera cet essai ouvert,
monocentrique, initié par un investigateur, destiné à évaluer
l'efficacité et la sécurité d'emploi de nitazoxanide chez des
patients atteints de fibrose de stade 2 ou 3 induite par la
NASH.
Les objectifs de cette étude
preuve de concept incluent l'évaluation de l'effet
anti-fibrotique de nitazoxanide grâce à différentes approches, dont
une méthode innovante permettant de quantifier les taux de
fibrogenèse hépatique. Grâce à un marquage à l'eau deutérée, le
taux de synthèse de novo de protéines
circulantes associées au collagène sera déterminé par la technique
FSR (Fractional Synthesis Rate) au début et à
la fin du traitement afin d'évaluer les effets de l'administration
quotidienne de nitazoxanide. D'autres méthodes non invasives, y
compris l'Élastographie à Résonnance Magnétique (ERM) et le
FibroScan® seront utilisées pour évaluer les variations de rigidité
du foie après le traitement par nitazoxanide.
Nitazoxanide, actuellement sur le
marché et prescrit aux États-Unis ainsi que dans d'autres
territoires comme médicament antiparasitaire, possède des
propriétés anti-fibrotiques découvertes par Genfit et confirmées,
depuis, dans des modèles précliniques de fibrose. Genfit a présenté
les résultats de ces recherches en avril 2017 à l'International
Liver Congress de l'European Association for the Study of the Liver
(EASL), démontrant l'efficacité de nitazoxanide dans des modèles
pathologiques in vivo de fibrose hépatique.
Genfit a constaté dans ces modèles que l'administration de
nitazoxanide atténuait de manière significative le développement
fibrotique. Des données précliniques supplémentaires ont été
présentées en avril 2018 à l'EASL portant sur des combinaisons de
traitements avec une faible dose d'elafibranor et de nitazoxanide.
Ces résultats indiquent que nitazoxanide pourrait être un bon
candidat en combinaison de traitement avec elafibranor ainsi qu'en
monothérapie antifibrotique.
Un brevet aux États-Unis a été
accordé à Genfit pour l'utilisation de nitazoxanide dans la fibrose
hépatique induite par la NASH.
Le Dr Stephen
Harrison du Pinnacle Clinical Research a déclaré :
« La découverte des effets anti-fibrotiques
de nitazoxanide par Genfit dans un modèle préclinique est
encourageante et pourra potentiellement apporter une nouvelle
possibilité de traitement intéressante pour les patients NASH
atteints de fibrose. J'ai hâte découvrir les résultats chez ces
patients et ainsi contribuer aux programmes de développement
prometteurs de Genfit pour nitazoxanide. »
Jean-François
Mouney, Président - Directeur Général de GENFIT, a ajouté :
« Nous sommes ravis du lancement de cette étude,
renforçant le pipeline de programmes cliniques de Genfit. Le Dr.
Harrison est un hépatologue de renommée internationale et un expert
dans la NAFLD et nous nous réjouissons de collaborer avec lui et le
Pinnacle Clinical Research pour mettre en oeuvre cette étude chez
des patients dont les besoins médicaux sont importants mais restent
non satisfaits. Nous sommes impatients de découvrir les résultats
de cette étude qui, s'ils sont positifs, permettront de continuer à
développer nitazoxanide pour le traitement de patients NASH à la
fois en monothérapie et en combinaison avec
elafibranor. »
À propos de la
NASH
La « NASH », ou
stéatohépatite non-alcoolique, est une maladie du foie qui associe
une accumulation de graisse dans le foie, une inflammation et une
dégénérescence des cellules hépatiques. La maladie est associée à
un risque élevé de progression vers la cirrhose, un état
correspondant à une fonction hépatique détériorée, conduisant à une
insuffisance hépatique et au cancer du foie.
À propos de
PINNACLE CLINICAL RESEARCH
Pinnacle Clinical Research est
engagé dans la conduite d'essais cliniques de phase avancée dans le
domaine de l'hépatologie et de la gastroentérologie, avec un
intérêt particulier pour la maladie du foie gras (fatty liver
disease). Le Pinnacle prône une recherche de haute qualité comme
complément à la prise en charge médicale courante des
volontaires.
À propos dE
GENFIT
GENFIT est une société
biopharmaceutique focalisée sur la découverte et le développement
de solutions thérapeutiques et diagnostiques visant les maladies du
foie, notamment d'origine métabolique, et les maladies
hépato-biliaires. GENFIT concentre ses efforts de R&D dans des
domaines thérapeutiques où les besoins médicaux sont considérables,
notamment en raison d'un manque de traitements approuvés.
Elafibranor, composé propriétaire le plus avancé de GENFIT, est un
candidat médicament actuellement en cours d'évaluation dans l'une
des études de phase 3 les plus avancées au monde (« RESOLVE-IT »)
dans la stéatohépatite non-alcoolique (NASH), pathologie considérée
comme une urgence médicale par les autorités réglementaires car
elle est silencieuse, potentiellement grave, et sa prévalence à
l'échelle mondiale est inquiétante. Ce composé est également en
cours d'évaluation dans une étude de phase 2 dans la Cholangite
Biliaire Primitive (PBC), une maladie hépatique rare. Dans le cadre
d'une approche intégrée de la prise en charge clinique des patients
NASH, GENFIT conduit en parallèle un programme de recherche et de
développement ayant pour but d'apporter aux patients et aux
praticiens un outil de diagnostic de la NASH basé sur un test de
diagnostic sanguin non invasif. Installée à Lille, Paris et
Cambridge, MA (USA), l'entreprise compte environ 150
collaborateurs. GENFIT est une société cotée sur le marché
réglementé d'Euronext à Paris, Compartiment B (Euronext : GNFT -
ISIN : FR0004163111). www.genfit.fr
AVERTISSEMENT
Ce communiqué de presse contient
des déclarations prospectives. Bien que la Société considère que
ses projections sont basées sur des hypothèses raisonnables, ces
déclarations prospectives peuvent être remises en cause par un
certain nombre d'aléas et d'incertitudes, ce qui pourrait donner
lieu à des résultats substantiellement différents de ceux décrits,
induits ou anticipés dans lesdites déclarations prospectives. Ces
aléas et incertitudes comprennent notamment les incertitudes
inhérentes à la recherche et développement, y compris dans le
domaine des biomarqueurs, au progrès et aux résultats d'essais
cliniques en cours et planifiés, aux examens et autorisations
d'autorités réglementaires comme la FDA et l'EMA de ces
candidats-médicaments et programmes de diagnostic concernant, au
succès d'une stratégie d'in-licensing, à la capacité de la Société
à maintenir, protéger et développer ses droits de propriétés
intellectuelle pour nitazoxanide sans enfreindre les droits
d'autres sociétés, à la capacité de la Société à continuer à lever
des fonds pour son développement, ainsi qu'à ceux développés à la
section 4 «Principaux Risques et incertitudes» du Document de
Référence enregistré par l'Autorité des marchés financiers (AMF) le
27 avril 2018 sous le numéro R.18-032 disponibles sur les sites
Internet de GENFIT (www.genfit.fr) et de l'AMF (www.amf-france.org)
et mis à jour dans son Rapport d'Activité et Financier Semestriel
au 30 Juin 2018 consultable dans la rubrique «Investisseurs» du
site internet de GENFIT. Sous réserve de la réglementation
applicable, la Société ne prend aucun engagement de mise à jour ou
de révision des informations contenues dans ce communiqué. Le
présent communiqué, et les informations qu'il contient, ne
constituent ni une offre de vente ou de souscription, ni la
sollicitation d'un ordre d'achat ou de souscription, des actions
GENFIT dans un quelconque pays. Ce communiqué de presse a été
réalisé en langues Française et Anglaise ; en cas de différence
entre les textes, la version française prévaudra.
Contact
GENFIT |
Investisseurs
Naomi EICHENBAUM - Relations
Investisseurs | Tel : +1 (617) 714 5252 | investors@genfit.com
RELATIONS
PRESSE | Media
Bruno ARABIAN - Ulysse
Communication | Tel : 06 87 88 47 26 |
barabian@ulysse-communication.com
Hélène LAVIN - GENFIT | Tel :
03 20 16 40 00 | helene.lavin@genfit.com
GENFIT | 885
Avenue Eugène Avinée, 59120 Loos - FRANCE | +333 2016 4000 |
www.genfit.com
2018.12.03 - Lancement NTZ - CP FR
-
This
announcement is distributed by West Corporation on behalf of West
Corporation clients.
The issuer of this announcement warrants that they are solely
responsible for the content, accuracy and originality of the
information contained therein.
Source: GENFIT via Globenewswire
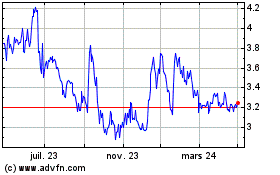
Genfit (EU:GNFT)
Graphique Historique de l'Action
De Mar 2024 à Avr 2024
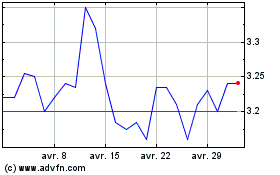
Genfit (EU:GNFT)
Graphique Historique de l'Action
De Avr 2023 à Avr 2024