Innate Pharma avance le programme de développement clinique de
lacutamab
Progression de l’essai TELLOMAK : la cohorte 2 de patients
présentant un mycosis fongoïde exprimant KIR3DL2 avance au stade 2
plus tôt que prévu
La Société initie deux nouveaux essais
cliniques pour évaluer lacutamab dans les lymphomes T
périphériques, dont un essai de Phase 2 en combinaison en
partenariat avec le groupe international de recherche sur les
lymphomes, LYSA
Une conférence avec des experts a lieu
aujourd’hui à 14h00 CET / 8h00 ET
Innate Pharma SA
(Euronext Paris : IPH – ISIN : FR0010331421 ; Nasdaq : IPHA)
(« Innate » ou la
« Société ») a annoncé aujourd'hui de
nouvelles avancées dans le développement clinique de son produit
expérimental propriétaire et « first-in-class »,
lacutamab. Lacutamab est un anticorps anti-KIR3DL2 en développement
dans les lymphomes à cellules T. Ces avancées concernent la
progression de la cohorte de patients présentant un mycosis
fongoïde exprimant KIR3DL2 (cohorte 2) au stade 2 dans l’étude
TELLOMAK, ainsi que l’initiation d’un programme clinique dans les
lymphomes T périphériques.
Mycosis fongoïdes : progression de la
cohorte 2 de l’essai TELLOMAK au stade 2 Dans l’étude de
Phase 2 TELLOMAK, une étude internationale, ouverte et
multi-cohorte, lacutamab a démontré un signal préliminaire positif
dans la cohorte 2. Cette cohorte a atteint le nombre pré-établi de
réponses nécessaires pour avancer au stade 2, permettant à la
Société de recruter des patients supplémentaires. La Société
prévoit de présenter ces données préliminaires en congrès
scientifique en 2021.
Le recrutement est en cours dans la cohorte 3,
qui évalue lacutamab en monothérapie chez les patients présentant
un mycosis fongoïde n’exprimant pas KIR3DL2.
Lymphomes T périphériques : initiation
d’une stratégie clinique basée sur les donnéesLa Société a
annoncé aujourd’hui qu’elle prévoit d’initier deux essais cliniques
en parallèle afin d’évaluer lacutamab chez les patients présentant
un lymphome T périphérique en rechute ou réfractaire et exprimant
KIR3DL2. Ensemble, ces essais permettront d’établir une stratégie
clinique basée sur les données afin d’identifier des opportunités
potentielles pour lacutamab dans les indications en rechutes, ainsi
qu’une possible extension future en traitement de premières lignes
dans les lymphomes T périphériques.
- Essai de Phase 1b : un essai clinique de Phase
1b sponsorisé par la Société, évaluant lacutamab en monothérapie
chez les patients présentant un lymphome T périphérique en rechute
et exprimant KIR3DL2.
- Essai de Phase 2 KILT1 : The
Lymphoma Study Association (LYSA) va mettre en place en tant
que promoteur un essai randomisé, évaluant lacutamab en combinaison
avec une chimiothérapie GEMOX (gemcitabine en combinaison avec
oxaliplatin) contre GEMOX seule chez les patients en rechute ou
réfractaires et exprimant KIR3DL2.
« Lacutamab est notre produit clinique
prioritaire, et nous sommes ravis de partager le progrès important
sur ce programme. Le signal préliminaire observé dans la population
de patients présentant un mycosis fongoïde exprimant KIR3DL2 est
encourageant et a conduit à franchir le seuil pré-établi pour cette
cohorte plus tôt que prévu, » commente Joyson
Karakunnel, MD, MSc, FACP, Directeur Médical d’Innate
Pharma. « De plus, nos essais dans les lymphomes T
périphériques annoncés aujourd’hui renforcent notre stratégie
d’évaluer le potentiel de lacutamab dans des indications en rechute
ou réfractaires dans un premier temps, puis potentiellement
d’étendre à des lignes de traitement plus en amont. Collaborer avec
l’association LYSA nous apportera une expertise d’une valeur
inestimable compte tenu de leur expérience dans l’établissement de
stratégies thérapeutiques pour les patients ayant un
lymphome. »
« Les patients présentant un lymphome T
périphérique en rechute ont grandement besoin d’options
thérapeutiques alternatives et efficaces, et nous sommes heureux de
collaborer avec Innate Pharma dans le cadre de cette étude, »
commente Franck Morschhauser, Professeur d’hématologie à
Lille et Président du groupe coopérateur LYSA. « KIR3DL2
est une cible significative dans la mesure où elle est exprimée
jusqu’à 50% des sous-types de lymphomes T périphériques. En nous
appuyant sur notre réseau international et notre expertise dans le
lymphome, nous pensons que cette étude va nous aider à mieux
comprendre le potentiel de lacutamab pour aider ces patients. »
Pour en savoir plus sur ces mises à jour, une
conférence virtuelle a lieu ce jour avec l’équipe de direction
d’Innate ainsi que le Professeur Pierluigi Porcu, Professeur
d’oncologie médicale, de dermatologie et de biologie cutanée,
Directeur de la division des maladies hématologiques et de
transplantation de cellules souches hématopoïétiques de
l’Université Thomas Jefferson de Philadelphie et investigateur
principal de l'essai clinique de Phase 2 TELLOMAK d'Innate, et le
Professeur Olivier Hermine, Professeur d'hématologie à l'Université
Paris Descartes, Chef du service d’hématologie adultes de l’Hôpital
Universitaire Necker Enfants Malades et investigateur
principal de l’étude de Phase 2 KILT menée par LYSA.
La conférence
virtuelle se tiendra aujourd’hui à 14h00 CET / 8h00 ET
Le direct de
l'événement sera disponible au lien suivant
:https://edge.media-server.com/mmc/p/yztsebvs
Un numéro de téléphone
est également mis à disposition. Pour cela, les participants
peuvent s'inscrire avant l'événement à l'adresse
http://emea.directeventreg.com/registration/2284358. Lors de leur
inscription, les participants recevront par e-mail le numéro
d'appel, un code d'accès direct à l'événement et un identifiant
unique qu'ils pourront utiliser 10 minutes avant le début de
l'événement pour y accéder.
Ces informations sont
également disponibles dans la rubrique investisseurs du site
internet d’Innate, www.innate-pharma.com. Une rediffusion sera
accessible dans la rubrique investisseurs du site d'Innate pendant
90 jours après l'événement.
À propos de lacutamab
:
Lacutamab (IPH4102) est un anticorps humanisé «
first-in-class » induisant la cytotoxicité, ciblant KIR3DL2
actuellement en cours d’évaluation clinique dans les
lymphomes T cutanés (LTC), une indication orpheline. Les LTC sont
un ensemble de lymphomes rares des lymphocytes T. Dans les stades
avancés de LTC, il existe peu d’options thérapeutiques et le
pronostic est défavorable.
KIR3DL2 est un récepteur inhibiteur de la
famille des KIR, exprimé par environ 65% des patients présentant un
LTC, pour l’ensemble des sous-types et stades de la maladie ; cette
fréquence augmente jusqu’à 90% des patients atteints de certains
LTC de mauvais pronostic, en particulier le syndrome de Sézary. Il
est exprimé par jusqu'à 50% des patients atteints de lymphome T
périphérique. Son expression est limitée dans les tissus sains.
À propos de l’étude TELLOMAK
:
TELLOMAK est une étude de Phase 2
internationale, ouverte, multi-cohorte, conduite aux Etats-Unis et
en Europe. Lacutamab y est évalué chez des patients présentant un
lymphome T avancé. Il est prévu de recruter jusqu’à 150 patients
pour évaluer lacutamab :
- en monothérapie chez 60 patients environ atteints d’un syndrome
de Sézary ayant reçu au moins deux traitements antérieurs, dont le
mogamulizumab,
- en monothérapie chez 90 patients environ atteints de mycosis
fongoïde (MF) ayant reçu au moins deux traitements antérieurs.
Chez les patients présentant un MF, l’étude est
conçue pour évaluer le bénéfice de lacutamab en fonction de
l’expression de KIR3DL2. L’étude inclut deux cohortes dans le MF,
testant lacutamab chez des patients exprimant et n’exprimant pas
KIR3DL2 respectivement. Ces cohortes suivent chacune un schéma en
deux étapes, et seront arrêtées après la première étape si le
traitement est jugé inutile. La cohorte du syndrome de Sézary de
l’étude pourrait sous certaines conditions permettre
l’enregistrement de lacutamab dans cette indication.
Le critère d'évaluation principal de l'essai est
le taux de réponse objective. Les critères secondaires incluent la
survie sans progression, la durée de la réponse, la qualité de vie
et l’incidence d’évènements indésirables liés au traitement.
À propos de lacutamab dans les lymphomes
T périphériques :
Deux essais cliniques porteront sur le lacutamab
chez des patients atteints de lymphomes T périphériques exprimant
KIR3DL2 et ayant reçu au moins un traitement systémique préalable.
Lacutamab sera évalué :
- Dans un essai clinique de Phase 1b multicentrique en
monothérapie chez environ 20 patients en rechute exprimant
KIR3DL2. L'essai est conçu pour évaluer la sécurité, ainsi que pour
caractériser les résultats cliniques, la pharmacocinétique et
l'immunogénicité de lacutamab en monothérapie dans le lymphome T
périphérique. D’autres développements seront déterminés sur la base
de signaux préliminaires d'efficacité.
- Dans un essai de Phase 2 multicentrique et randomisé en
combinaison avec GEMOX chez des patients en rechute/réfractaires
exprimant KIR3DL2. Cette étude comprendra environ 60 patients.
L'essai combiné, KILT (anti-KIR dans le lymphome à cellules T), est
mené par The Lymphoma Study Association (LYSA) et par sa structure
opérationnelle (LYSARC). Elle évaluera l'efficacité et la sécurité
de lacutamab en combinaison avec une chimiothérapie GEMOX chez des
patients pré screenés, avec la survie sans progression comme
critère d'évaluation principal.
À propos d’Innate Pharma :
Innate Pharma S.A. est une société de
biotechnologies au stade clinique, spécialisée en immuno-oncologie
et dédiée à l’amélioration du traitement des cancers grâce à des
anticorps thérapeutiques innovants exploitant le système
immunitaire.
Le large portefeuille d’anticorps d’Innate
Pharma inclut plusieurs candidats potentiellement
« first-in-class » aux stades clinique et préclinique dans des
cancers où le besoin médical est important.
Innate Pharma est pionnière dans la
compréhension de la biologie des cellules NK et a développé son
expertise dans le microenvironnement tumoral et les antigènes
tumoraux, ainsi que dans l'ingénierie des anticorps. Son approche
innovante lui a permis de construire un portefeuille propriétaire
diversifié et de nouer des alliances avec des sociétés leaders de
la biopharmacie comme Bristol-Myers Squibb, Novo Nordisk A/S ou
Sanofi ainsi qu’un partenariat multi-produits avec AstraZeneca.
Basée à Marseille avec une filiale à Rockville
(Maryland, Etats-Unis), Innate Pharma est cotée en bourse sur
Euronext Paris et sur Nasdaq aux Etats-Unis.
Retrouvez Innate Pharma sur
www.innate-pharma.com.
Informations
pratiques :
|
Code ISINCode
mnémoniqueLEI |
FR0010331421Euronext : IPH Nasdaq : IPHA9695002Y8420ZB8HJE29 |
Avertissement concernant les
informations prospectives et les facteurs de risques :
Ce communiqué de presse contient des
déclarations prospectives, y compris celles au sens du Private
Securities Litigation Reform Act de 1995. L'emploi de certains
termes, notamment « croire », « potentiel »,
« s'attendre à » et « sera » et d'autres
expressions semblables, vise à identifier des énoncés prospectifs.
Bien que la Société considère que ses projections sont basées sur
des hypothèses raisonnables, ces déclarations prospectives peuvent
être remises en cause par un certain nombre d’aléas et
d’incertitudes, ce qui pourrait donner lieu à des résultats
substantiellement différents de ceux anticipés. Ces aléas et
incertitudes comprennent notamment les incertitudes inhérentes à la
recherche et développement, y compris celles relatives à
l’innocuité, aux progrès et aux résultats des essais cliniques et
des études précliniques en cours ou prévus, aux examens et
autorisations d’autorités réglementaires concernant les
produits-candidats de la Société, des efforts commerciaux de la
Société, la capacité de la Société à continuer à lever des fonds
pour son développement et l’impact global de la pandémie de
COVID-19 sur les systèmes de santé ainsi que les activités, la
situation financière et les résultats de la Société. Pour des
considérations supplémentaires en matière de risques et
d’incertitudes pouvant faire différer les résultats effectifs, la
situation financière, la performance et les réussites de la
Société, merci de vous référer à la section « Facteurs de Risques »
du Document d’Enregistrement Universel déposé auprès de l’Autorité
des marchés financiers (AMF), disponible sur les sites Internet
d’Innate Pharma (www.innate-pharma.com) et de l’AMF
(www.amf-france.org), et les documents et rapports publics déposés
auprès de la Securities and Exchange Commission (SEC) des
États-Unis, y compris le rapport annuel sur « Form 20-F »
pour l’exercice clos le 31 décembre 2019 et les documents et
rapports subséquents déposés auprès de l'AMF ou de la SEC, ou
autrement rendus publics, par la Société.
Le présent communiqué, et les informations qu’il
contient, ne constituent ni une offre de vente ou de souscription,
ni la sollicitation d’un ordre d’achat ou de souscription, des
actions d’Innate Pharma dans un quelconque pays.
Pour tout renseignement complémentaire,
merci de contacter :
|
Relations investisseurs
|
Contacts Presse |
|
Innate Pharma |
Innate Pharma |
|
Tel.: +33 (0)4 30 30 30 30investors@innate-pharma.com |
Tracy Rossin (Global / US)Tel. : +1 240 801
0076Tracy.Rossin@innate-pharma.com |
|
|
ATCG Press Marie Puvieux (France)Tel. : +33 (0)9
81 87 46 72innate-pharma@atcg-partners.com |
1 anti-KIR dans le lymphoma à cellules T
- Lacutamab PR FR Feb 9 final
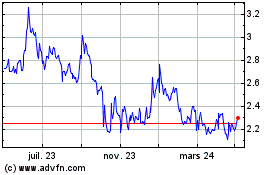
Innate Pharma (EU:IPH)
Graphique Historique de l'Action
De Mar 2024 à Avr 2024
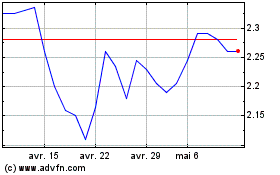
Innate Pharma (EU:IPH)
Graphique Historique de l'Action
De Avr 2023 à Avr 2024