L’accord avec la Fondation Bill & Melinda Gates prévoit
que MedinCell conserve les droits commerciaux du produit dans le
monde entier, notamment aux États-Unis.
Regulatory News:
Ce communiqué de presse contient des éléments
multimédias. Voir le communiqué complet ici :
https://www.businesswire.com/news/home/20191128005501/fr/
MedinCell Human Health Portfolio,
September 2019 (Graphique: MedinCell)
MedinCell (Paris:MEDCL) et la Fondation Bill & Melinda
Gates ont signé un accord pour une subvention supplémentaire
représentant une enveloppe totale de 19 millions de dollars sur
quatre ans. Elle vise à financer les activités précliniques et les
études cliniques de phase 1 d’un contraceptif injectable
biorésorbable actif sur une durée de six mois (mdc-WWM). La
subvention est structurée sous la forme d’avances sur les coûts
engendrés par le projet, versées par tranches. Selon les options
choisies et en fonction des avancées du programme, jusqu’à 11,75
millions de dollars pourraient être perçus sur les 12 prochains
mois, incluant un premier versement immédiat de 4,75 millions de
dollars. Les 7,25 millions de dollars restants pourront être perçus
ultérieurement.
Pour mémoire, une précédente subvention de 3,5 millions de
dollars accordée en novembre 2017 par la Fondation Gates finance la
phase de recherche de formulation du produit. Ses résultats
complets devraient permettre de sélectionner la formulation
candidate.
MedinCell conserve les droits de commercialisation du produit
dans le monde, notamment aux États-Unis où le marché de la
contraception pesait plus de 5 milliards de dollars en 2018. Les
contraceptifs réversibles à longue durée d'action (CRLDA),
essentiellement les implants solides et les dispositifs
intra-utérins, représentaient à eux seuls 28% de ce marché, soit
plus de 1,4 milliard de dollars, avec une croissance annuelle
moyenne de 7,8% sur les 5 dernières années. Le produit mdc-WWM
pourrait prendre une part significative de ce marché et même
l’élargir en facilitant l’adoption et l’utilisation de ce type de
contraception1.
Conformément à leur stratégie de Global Access et afin
d’avoir un réel impact dans la vie des femmes, les deux partenaires
prévoient de rendre le produit largement disponible. Des prix
abordables dans les économies en développement permettront
d’éliminer la barrière du prix et de favoriser l’adoption
volontaire du produit. L’intérêt marqué des femmes et jeunes femmes
pour la contraception à longue durée d'action présage du fort
potentiel de croissance du marché au bénéfice de la santé des
femmes, des nouveau-nés et des enfants. La Fondation Gates dispose
également d’une licence non exclusive pour une utilisation
non-commerciale du produit dans les pays à revenu faible ou
intermédiaire.
mdc-WWM pourrait être le premier contraceptif à réunir les
caractéristiques essentielles pour devenir une référence dans les
pays en développement et dans les pays développés : molécule
progestative (non MPA), 6 mois d’action, injection sous-cutanée,
dépôt entièrement biorésorbable, accessibilité du traitement.
La Fondation Gates soutient le développement de produits visant
à améliorer la santé des populations les plus vulnérables du monde.
Environ 74 millions de femmes tombent enceintes involontairement
chaque année, entraînant 25 millions d’interruptions volontaires de
grossesse à risque et 47 000 décès2. Améliorer l'accès à une
contraception efficace - accompagnée d’une information claire et de
services pertinents en matière de planning familial - vise à
réduire le nombre de grossesses non désirées et les décès qui en
résultent, ainsi qu’à faire baisser les taux d'avortement et le
nombre de décès infantiles. Améliorer l’accès à la contraception
est donc un réel enjeu de santé publique pouvant favoriser les
impacts économiques et culturels.
mdc-WWM pourrait en effet répondre à plusieurs défis majeurs
tels que le cout de la contraception, l’insuffisance des réseaux de
distribution ou encore certaines barrières culturelles.
Contrairement à la plupart des autres contraceptifs réversibles à
longue durée d'action tels que les implants, aucune intervention
chirurgicale ou spécialisée ne sera nécessaire avec le produit
développé par MedinCell. Une simple injection sous-cutanée forme un
dépôt de quelques millimètres qui agit comme une pompe virtuelle
pendant 6 mois avant de disparaitre complètement. Des études ont
montré que le risque d'échec de contraception chez les femmes
suivant un traitement contraceptif oral ou via d'autres méthodes
était 17 à 20 fois plus élevé qu’avec l’utilisation d’un
contraceptif réversible à longue durée d'action, essentiellement en
raison du manque d'observance3.
mdc-WWM serait le sixième produit de MedinCell à rentrer en
développement. Tous utilisent des principes actifs déjà approuvés
ayant démontré leur innocuité et leur efficacité, augmentant de
manière significative les chances de succès.
_______________________________________________________________________________________________________________________________________________________________________________________________
Actualités MedinCell sur les 12 derniers mois
(communiqués de presse disponibles sur invest.medincell.com)
Le programme mdc-CWM progresse comme prévu - 25 septembre
2019
L’Assemblée Générale de MedinCell vote l’inscription de la
raison d’être de la société dans ses statuts - 10 septembre
2019
Subvention de la Fondation Gates pour développer un traitement
injectable à action prolongée pour la prévention du VIH (PrEP) - 5
septembre 2019
Nouvelle association pour exploiter le potentiel financier de sa
technologie dans la santé animale - 28 août 2019
Feu vert de la FDA pour démarrer les essais cliniques d’un
antipsychotique injectable à action prolongée -26 août 2019
Encaissement de 7,5 M€ de la Banque Européenne d’Investissement
(BEI) - 23 juillet 2019
Entrée en développement préclinique d’un troisième traitement
antipsychotique injectable à action prolongée - 9 juillet 2019
Trophée #LetsgoFrance 2019 dans la catégorie « France, un modèle
d’économie durable » - 5 avril 2019
Démonstration in vivo de l’efficacité du premier injectable
combinant anesthésie chirurgicale et traitement de la douleur
postopératoire sans opioïde - 11 mars 2019
Encaissement la deuxième partie de la subvention de la Fondation
Bill & Melinda Gates - 24 janvier 2019
Succès de l’introduction en bourse - 3 octobre 2018
_______________________________________________________________________________________________________________________________________________________________________________________________
A propos de MedinCell
MedinCell est une société pharmaceutique technologique au stade
clinique qui développe un portefeuille de produits injectables à
action prolongée dans différentes aires thérapeutiques en associant
sa technologie propriétaire BEPO® à des principes actifs déjà
connus et commercialisés. MedinCell, à travers la libération
contrôlée et prolongée du principe actif, rend les traitements
médicaux plus efficients grâce notamment à l’amélioration de
l’observance, c’est-à-dire le respect des prescriptions médicales,
et à la diminution significative de la quantité de médicament
nécessaire dans le cadre d’un traitement ponctuel ou chronique. La
technologie BEPO® permet de contrôler et de garantir la délivrance
régulière à dose thérapeutique optimale d’un médicament pendant
plusieurs jours, semaines ou mois à partir de l’injection
sous-cutanée ou locale d’un simple dépôt de quelques millimètres,
entièrement biorésorbable. Basée à Montpellier, MedinCell compte
actuellement plus de 130 collaborateurs de plus de 25 nationalités
différentes.
www.medincell.com
_______________________________________________________________________________________________________________________________________________________________________________________________
Ce communiqué de presse peut contenir des déclarations
prospectives, notamment concernant la progression des essais
cliniques de la Société. Même si la Société considère que ses
prévisions sont fondées sur des hypothèses raisonnables, toutes
déclarations autres que des déclarations de faits historiques que
pourrait contenir ce communiqué de presse relatives à des
événements futurs sont sujettes à des changements sans préavis, à
des facteurs que la Société ne maîtrise pas et aux capacités
financières de la Société.
Ces déclarations peuvent inclure, sans que cette liste soit
limitative, toutes déclarations commençant par, suivies par ou
comprenant des mots ou expressions tels que « objectif », « croire
», « prévoir », « viser », « avoir l’intention de », « pouvoir », «
anticiper », « estimer », « planifier », « projeter », « devra », «
peut avoir », « probablement », « devrait », « pourrait » et
d’autres mots et expressions de même sens ou employés à la forme
négative. Les déclarations prospectives sont sujettes à des risques
intrinsèques et à des incertitudes hors du contrôle de la Société
qui peuvent, le cas échéant, entraîner des différences notables
entre les résultats, performances ou réalisations réels de la
Société et ceux anticipés ou exprimés explicitement ou
implicitement par lesdites déclarations prospectives.
Une liste et une description de ces risques, aléas et
incertitudes figurent dans les documents déposés par la société
auprès de l’Autorité des Marchés Financiers (AMF) au titre de ses
obligations réglementaires, y compris dans le document de base de
la Société, enregistré auprès de l’AMF le 4 septembre 2018 sous le
numéro I. 18-062, ainsi que dans les documents et rapports qui
seront publiés ultérieurement par la Société. Par ailleurs, ces
déclarations prospectives ne valent qu’à la date du présent
communiqué de presse. Les lecteurs sont invités à ne pas se fier
indûment à ces déclarations prospectives. Sauf exigence légale, la
Société ne reconnaît aucune obligation de mettre à jour
publiquement ces déclarations prospectives, ni d’actualiser les
raisons pour lesquelles les résultats avérés pourraient varier
sensiblement des résultats anticipés par les déclarations
prospectives, et ce y compris dans le cas où des informations
nouvelles viendraient à être disponibles. La mise à jour par la
Société d’une ou plusieurs déclarations prospectives n’impliquera
pas qu’elle procédera ou non à d’autres actualisations de ces
déclarations prospectives ou d’autres déclarations
prospectives.
Ce communiqué de presse est publié à des fins d’information
uniquement. Les informations qu’il contient ne constituent ni une
offre de vente, ni une sollicitation d’offre d’achat ou de
souscription de titres de la Société dans quelque juridiction que
ce soit, en particulier en France. De la même façon, ce communiqué
ne constitue pas un conseil en investissement et ne saurait être
traité comme tel. Il n’a aucun lien avec les objectifs
d’investissement, la situation financière ou les besoins
spécifiques d’un quelconque destinataire. Il ne saurait priver les
destinataires d’exercer leur propre jugement. Toutes les opinions
exprimées dans ce document sont sujettes à modification sans
préavis. La diffusion de ce communiqué de presse peut être encadrée
par des dispositions restrictives du droit dans certaines
juridictions. Les personnes qui viendraient à prendre connaissance
du présent communiqué de presse sont tenues de se renseigner quant
à ces restrictions et de s’y conformer.
1 Source : IQVIA 2 Source : OMS - oct. 2019 3 Winner, B;
Peipert, JF; Zhao, Q; Buckel, C; Madden, T; Allsworth, JE; Secura,
GM. (2012), “Effectiveness of Long-Acting Reversible
Contraception”, New England Journal of Medicine, 366 (21):
1998–2007, doi:10.1056/NEJMoa1110855, PMID 22621627
Consultez la
version source sur businesswire.com : https://www.businesswire.com/news/home/20191128005501/fr/
MedinCell David
Heuzé Communication
leader david.heuze@medincell.com +33 (0)6 83 25 21 86
NewCap Louis-Victor
Delouvrier / Alexia Faure Relations investisseurs
medincell@newcap.eu +33 (0)1 44 71 94 94
NewCap Nicolas
Merigeau Relations
médias medincell@newcap.eu +33 (0)1 44 71 94 94
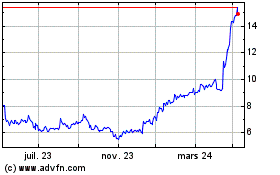
Medincell (EU:MEDCL)
Graphique Historique de l'Action
De Mar 2024 à Avr 2024
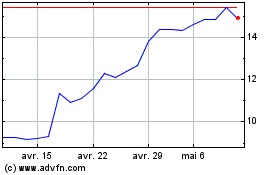
Medincell (EU:MEDCL)
Graphique Historique de l'Action
De Avr 2023 à Avr 2024