Actualisé: Le vaccin de Valneva contre le chikungunya approuvé aux USA, le titre bondit
10 Novembre 2023 - 11:50AM
Dow Jones News
(Actualisation: précisions sur l'autorisation de la FDA et sur la
mise en vente du bon de revue prioritaire, commentaires d'analyste,
cours de Bourse)
PARIS (Agefi-Dow Jones)--L'action Valneva bondit vendredi, alors
que la Food and Drug Administration (FDA), l'autorité sanitaire
américaine, a approuvé son candidat-vaccin contre le chikungunya,
VLA1553.
A 11h30, le titre gagnait 9%, à 6,88 euros, soit la plus forte
hausse au sein du SBF 120.
Le vaccin, commercialisé sous le nom d'Ixchiq, a été autorisé aux
Etats-Unis pour les personnes de 18 ans et plus présentant un
risque accru d'être exposées au virus, a indiqué Valneva dans un
communiqué. Ce vaccin unidose contient le virus atténué, une
technique classique utilisée pour d'autres vaccins.
"Cette décision constitue une excellente nouvelle pour Valneva
après la déconvenue de son vaccin Covid", a commenté Mohamed
Kaabouni, analyste chez Portzamparc, qui a souligné que cette
décision de la FDA représentait le principal catalyseur du titre à
court terme.
Dans ce cadre, l'intermédiaire financier a relevé son objectif de
cours sur le titre de 10,10 euros à 11 euros et a maintenu sa
recommandation "acheter".
L'Ixchiq est le premier vaccin autorisé au monde contre le
chikungunya, un marché estimé à plus de 500 millions de dollars par
an d'ici à 2032, a rappelé l'analyste.
Valneva prévoit de commencer à commercialiser le vaccin aux
Etats-Unis au début de l'année prochaine.
Une demande d'autorisation a également été déposée par Valneva
auprès de l'Agence européenne des médicaments (EMA) et de Santé
Canada.
Par ailleurs, le groupe a confirmé son intention de vendre le bon
de revue prioritaire (PRV) qu'il a reçu de la FDA afin de le
récompenser de ses recherches pour répondre à un besoin médical non
satisfait.
"Cette transaction est courante chez les biotechs. Elle permettra à
Valneva de renforcer sa trésorerie et de financer ses programmes de
recherche et de développement (R&D)", a précisé Mohamed
Kaabouni.
Les grands laboratoires sont friands de ces bons de revue de la
FDA, assimilables à des "passe-droits". Ils garantissent que
l'autorité sanitaire américaine étudiera en priorité le dossier
d'autorisation de mise sur le marché déposé par le détenteur du
bon.
"Détenir un bon de revue prioritaire permet d'avancer de plusieurs
mois la commercialisation d'un produit, soit de gagner
potentiellement des dizaines de millions de dollars
supplémentaires", a souligné Mohamed Kaabouni, qui a ajouté que ces
bons se négociaient autour de 100 millions de dollars l'unité.
-Pierre-Jean Lepagnot, Agefi-Dow Jones; +33 (0)1 41 27 47 95;
pjlepagnot@agefi.fr ed: LBO
Agefi-Dow Jones The financial newswire
(END) Dow Jones Newswires
November 10, 2023 05:30 ET (10:30 GMT)
Copyright (c) 2023 L'AGEFI SA
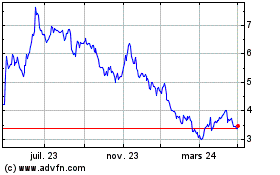
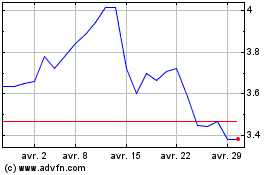
Valneva (EU:VLA)
Graphique Historique de l'Action
De Juin 2024 à Juil 2024
Valneva (EU:VLA)
Graphique Historique de l'Action
De Juil 2023 à Juil 2024